Bảng Tuần Hoàn Lớp 8 - Bảng Tuần Hoàn Hóa Học Lớp 8 Trang 42
Chào những bạn, tôi là admin trang web này, tôi đã giỏi nghiệp đh ngành công nghệ thông tin. 3 môn tôi thi đại học là Toán, thứ Lý và Hóa Học… Tôi chỉ đạt mức 3 điểm cho môn hóa học với đề thi trắc nghiệm hóa học cơ mà thôi.
Bạn đang xem: Bảng tuần hoàn lớp 8
Tại sao tôi vẫn đỗ đại học, à môn toán của tớ được 8 điểm lận, môn toán đã cứu vớt vớt đời tôi. Cũng chính vì thế tôi làm website này cùng truyền đạt cho các bạn là môn chất hóa học nó khó như thế nào. Các bạn đã bước đầu vào lớp 8 bạn đã được học hóa, vậy hãy cẩn thận với các kiến thức gốc rễ hóa học tập lớp 8 này nhé. Vì nếu mất nơi bắt đầu môn hóa thì sẽ y hệt như tôi đó, lên lớp 12 ngồi nghe cô giảng nhưng chẳng hiểu gì.
Bảng tuần hoàn chất hóa học lớp 8 là gì? Hiểu đơn giản dễ dàng thôi nó liệt kê cho bạn 20 nguyên tố hóa học thân quen nhất, các bạn sẽ gặp nó suốt những năm sau này. Bởi vì thế hãy làm cho quen, à quên chúng ta phải học tập thuộc lòng nó bắt đầu phải. Học thuộc cả các thứ tương quan đến bọn chúng như ký kết hiệu, hóa trị, số hiệu nguyên tử, nguyên tử khối…
Bạn buộc phải nhớ kỹ cái biển này càng cấp tốc càng tốt. Vì bạn sẽ gặp nó trong bài xích tập, bài xích thi, tất cả 30% các câu hỏi trong kỳ thi cuối kỳ mà bạn chỉ cần hiểu thật kỹ càng 20 yếu tố này là đã trả lời được rồi.
Bảng tuần trả hóalớp 8 trang 42
-
| hydro | 1 | H | 1 | I | |
| heli | 2 | He | 4 | ||
| liti | 3 | Li | 7 | I | |
| beri | 4 | Be | 9 | II | |
| bo | 5 | B | 11 | III | |
| cacbon | 6 | C | 12 | IV, II | |
| nito | 7 | N | 14 | II, III, IV… | |
| oxy | 8 | O | 16 | II | |
| flo | 9 | F | 19 | I | |
| neon | 10 | Ne | 20 | ||
| natri | 11 | Na | 23 | I | |
| magie | 12 | Mg | 24 | II | |
| nhom | 13 | Al | 27 | III | |
| silic | 14 | Si | 28 | IV | |
| photpho | 15 | P | 31 | III, V | |
| lưu huỳnh | 16 | S | 32 | II, IV, VI | |
| clo | 17 | Cl | 35.5 | I,… | |
| argon | 18 | Ar | 39.9 | ||
| kali | 19 | K | 39 | I |
Cơ sở thực thụ của bảng tuần trả hóa họclớp 8
-
Bảng tuần hoàn bọn họ sử dụng thời buổi này dựa nằm trong bảng tuần hoàn vày Dmitri Mendeleev phát minh sáng tạo và chào làng vào năm 1869.
Mendeleev nhận biết rằng ông rất có thể sắp xếp 65 nguyên tố vẫn biết vào một bảng làm sao để cho mỗi bộ phận có:
1.Khối lượng nguyên tử khủng hơn khối lượng nguyên tố nằm cạnh sát trái của nó. Ví dụ, magie (trọng lượng nguyên tử 24,3) được đặt bên buộc phải của natri (trọng lượng nguyên tử 23,0).
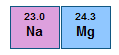
Năm 1913, hóa học với vật lý trở nên rối ren. Một trong những nhà khoa học lớn - bao hàm Mendeleev - vẫn nói chuyện tráng lệ và trang nghiêm về các nguyên tố nhẹ hơn hydro và các nguyên tố nằm trong lòng hydro và heli. Hình dung về nguyên tử và biện minh của Mendeleev cho 1 bảng tuần hoàn dựa trên trọng lương nguyên tử đang được sản xuất ra.
2.Tính hóa học hóa học giống như trong cùng một cột. Hay nói theo một cách khác là phản bội ứng hóa học tương tự. Ví dụ, magie được xếp vào cột kiềm thổ, thuộc với những nguyên tố khác gồm cùng phản ứng tương tự là Be, Sr.

Mendeleev phân biệt rằng bảng tuần hoàn đang là trọng tâm của môn hóa học. Và hơn thế nữa nữa, Mendeleev thấy rằng bảng tuần trả của ông chưa hoàn thành và dự báo các khoảng trống và đặc thù phải có của những nguyên tố còn thiếu trong bảng tuần hoàn tương lai.
Cũng giống hệt như Adams với Le Verrier hoàn toàn có thể được xem như là phát chỉ ra hành tinh Neptune trên giấy. Mendeleev được coi là phát hiện ra germanium trên giấy. Ông hotline tên nguyên tố new này là eka-silicon, sau thời điểm quan gần cạnh thấy không gian trong bảng tuần hoàn giữa silicon cùng thiếc:

Tương tự, Mendeleev cũng phát hiển thị gali (eka-aluminum) và scandium (eka-boron) trên lý thuyết. Chính vì ông đã dự kiến sự mãi mãi và đặc điểm của chúng trước lúc chúng đích thực được tra cứu ra.
Xem thêm: Nước cốt dừa thái lan - nước cốt dừa thai coconut opera lon 165ml
Mặc dù Mendeleev đã tạo nên một bước nâng tầm quan trọng, tuy thế ông vẫn có những suy luận không nên lầm. Mendeleev đã có niềm tin rằng các đặc điểm hóa học tập được khẳng định bởi trọng lượng nguyên tử. Tất nhiên điều này trọn vẹn hợp lý với các kiến thức chất hóa học vào thời khắc đó.
27 năm sau thời gian của bảng tuần trả đầu tiên, electron với được phân phát hiện. Và mất 44 năm để tìm lời lý giải đúng cho bản chất của bảng tuần hoàn Mendeleev…
Chúng ta vẫn học gì ở chất hóa học lớp 8
-
Lớp 8 bọn họ sẽ bắt đầu học môn hóa học cùng sẽ ban đầu làm thân quen với bảng tuần hoàn nguyên tố hóa học. Vày hóa học gồm độ tinh vi cao với khá khó khăn để tưởng tượng nên ko được đào tạo ở lớp 7.
Ở đầu công tác hóa học tập lớp 8 bọn họ sẽ ban đầu làm thân quen với những khái niệm chất hóa học cơ phiên bản nhất và cơ chế thí nghiệm. Con kiến thức nền tảng gốc rễ hóa học lớp 8 rất đặc biệt vì nó là cơ sở để chúng ta học xuất sắc cho các năm sau. Chính vì như vậy hãy triệu tập cho kỹ nhé, hóa học là 1 trong những trong các môn rất đặc biệt quan trọng sau này bởi nó thông dụng để thi vào ngôi trường chuyên cung cấp 3 tốt xa hơn cùng đại học.
Các loài kiến thức thịnh hành ở chất hóa học lớp 8 là:
-
Tôi liệt kê cho chính mình tóm tắt các kiến thức mà bạn sẽ được học tập ở hóa lớp 8. Hoàn toàn có thể thấy đây phần đông là các kiến thức nền tảng, dạng học thuộc ko cần tính toán quá nhiều. Bài toán học giỏi các kiến thức căn cơ này sẽ giúp bạn học giỏi ở những năm tiếp theo. Hóa Học là một trong môn khôn xiết khó, rất nặng lý thuyết, có nhiều thứ chúng ta phải học tập thuộc như hóa trị, số hiệu nguyên tử, bảng tuần hoàn, độ hòa tan, độ bạo phổi yếu của kim loại... Nó càng quan trọng đặc biệt hơn là môn chủ yếu để thi lên cấp cho 3 tốt thi đại học.
Chương 1: chất – Nguyên Tử - Phân Tử
Chương 2: làm phản Ứng Hóa Học
Chương 3: Mol và đo lường Hóa Học
Chương 4: Oxi – không Khí
Chương 5: Hidro – Nước
Chương 6: Dung Dịch
Có thể thấy kiến thức và kỹ năng hóa học tập lớp 8 chỉ gồm các kiến thức solo giản. Nhưng cũng tương đối nặng nằn nì với 45 bài học xuyên thấu trong 6 chương. Tôi khuyên bạn nên tập trung còn nếu như không muốn mất loài kiến thức căn cơ của một môn học quan trọng đặc biệt nhất trong cả cấp 2 và cung cấp 3.
Bảng nguyên tố chất hóa học lớp 8 có ý nghĩa vô cùng đặc biệt trong chương trình huấn luyện và giảng dạy bộ môn Hóa học. Có nhiều nguyên tố khác biệt trong bảng, mỗi nguyên tố hoặc nhóm nguyên tử sẽ sở hữu những hóa trị riêng. Cùng tham khảo bài viết dưới trên đây để hiểu thêm về nguyên tố chất hóa học lớp 8 nhé.
1. Bảng Nguyên Tố hóa học Lớp 8 – Hóa trị của một số chất thường xuyên gặp
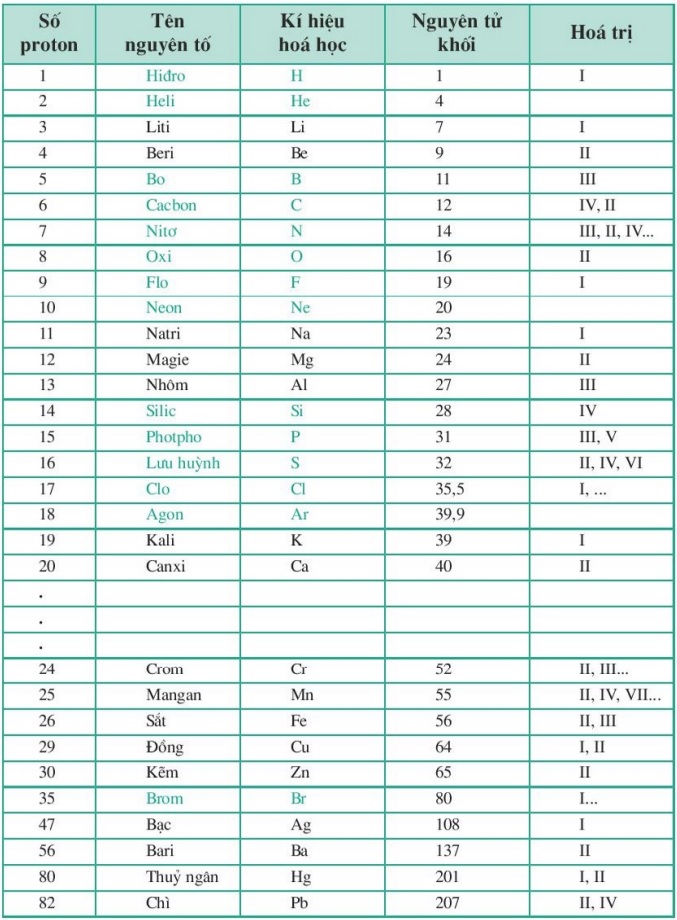
Bảng nguyên tố hóa học 8 tất cả có các thông tin về Số Proton, tên, ký kết hiệu hóa học, nguyên tử khối cùng hóa trị của nguyên tố nắm thể. Trong bảng sẽ bao gồm 30 nguyên tố hóa học thường lộ diện trong chương trình học chất hóa học lớp 8. Vậy nguyên tố chất hóa học lớp 8 là gì? Hóa trị của một số trong những chất thường gặp mặt là bao nhiêu?

Hóa trị của tập thể nhóm nguyên tử vào bảng nguyên tố hóa học lớp 8.
3. Bài ca hóa trị – Mẹo nhớ cấp tốc hóa trị của những nguyên tố chất hóa học lớp 8
Phần mập học sinh đều thấy khó khăn trong câu hỏi ghi lưu giữ hóa trị lúc được học tập về bảng nguyên tố hóa học lớp 8. Mặc dù nhiên, có khá nhiều mẹo nhằm giúp họ học ghi nhớ một cách dễ dàng và đơn giản và dễ dàng hiểu trải qua các bài bác ca hóa trị. Dưới đó là 1 bài ca hóa trị thông dụng nhưng các bạn cũng có thể tham khảo:
“Kali, Iot, Hidro
Natri cùng với Bạc, Clo một loài
Có hóa trị một các bạn ơi
Nhớ ghi mang lại rõ kẻo rồi phân vân
Magie, Chì, Kẽm, Thủy ngân
Canxi, Đồng ấy cũng xấp xỉ Bari
Cuối cùng thêm chú Oxi
Hóa trị hai ấy tất cả gì nặng nề khăn
Bác Nhôm hóa trị cha lần
Ghi sâu tâm trí khi cần phải có ngay
Cacbon, Silic này đây
Là hóa trị tứ không ngày nào quên
Sắt kia kể cũng thân quen tên
Hai, tía lên xuống thật phiền lắm thay
Nitơ trắc trở nhất đời
Một, hai, ba, bốn khi vậy nên năm
Lưu huỳnh lắm khi thi đấu khăm
Lúc hai, lúc bố khi nằm máy tư
Photpho nói tới không dư
Nếu ai hỏi đến thì ừ rằng năm
Bạn ơi cố gắng học chăm
Bài ca hóa trị trong cả năm khôn xiết cần.”
4. Kết luận
Bài viết trên phía trên của cửa hàng chúng tôi nhằm cung cấp thêm những kỹ năng và kiến thức hữu ích về bảng nguyên tố hóa học lớp 8. Để tất cả một nền tảng vững chắc về môn Hóa học, chúng ta học sinh buộc phải hiểu và học thuộc rất nhiều hóa trị cùng nguyên tử khối của các nguyên tố thường gặp gỡ cùng đội nguyên tử trên.
Chúc chúng ta đọc sẽ sở hữu được trải nghiệm tuyệt vời khi tham khảo bài viết này!
=>> các bạn hãy theo dõi kiến Guru để update bài giảng và kiến thức những môn học khác nhé!









